In der Ebene liegt ein
σ-Gerüst
vor.
Zwei
sp2-Orbitale von C überlappen;
Jeweils zwei sp2-Orbitale
von C
überlappen mit den 1s-Orbitalen von H.
| Kovalente Bindung |
IV.
Übungen |
|||
| Doppelbindung |
||||
Doppelbindungen, die von einem C-Atom ausgehen:
Eine Doppelbindung C = H ist unmöglich, weil H nur eine Bindung (durch Überlappung mit seinem 1s-Orbital) ausbilden kann.
Eine C = C Doppelbindung wird durch die sp2-Hybridisierung erklärt.
Ein C-Atom enthält damit drei sp2- Hybridorbitale und 1 p-Atomorbital. Das p-Orbital
steht senkrecht zur Ebene der drei sp2-Orbitale.
(Betrachten
Sie dazu die Herleitung: 2 p-Orbitale wurden für die Hybridisierung benutzt,
das 3. p-Orbital muss daher senkrecht auf diesen beiden stehen. Meistens definiert
man: px und py für die Hybridisierung benutzt und
pz als übrig bleibendes Orbital.)
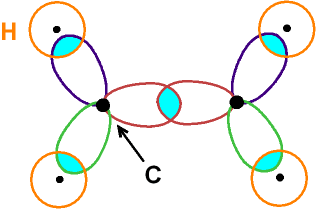
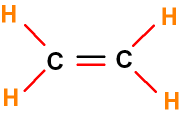
Als Beispiel das Molekül H2C = CH2
(Ethen)
Bei den Hybridorbitalen
ist jeweils nur die größere Hälfte skizziert!
|
In der Ebene liegt ein
σ-Gerüst
vor. |
|
|
|
|
|
|
|
Senkrecht zur Ebene |
|
|
Zwischen beiden C-Atomen liegen eine σ-Bindung aus der Überlappung sp2 mit sp2 und eine π-Bindung aus der Überlappung p mit p vor. Die zwei Bindungen sind in der Strichformel durch einen Doppelstrich gekennzeichnet. Die π-Bindung kann nur zusammen mit der σ-Bindung gebildet werden. Daher sagt man vereinfacht, eine Doppelbindung ist eine π-Bindung.
Bei Bindungen zu Heteroatomen C = O und C = N liegt die gleiche Bindungsart wie bei C = C - Bindungen vor.
Das σ-Gerüst allein würde freie Drehbarkeit erzeugen. Bei einer Verdrehung brechen aber die p-p-Überlappungen der π-Bindung auf. Da die Überlappung einen Energiegewinn liefert und dieser bei der Drehung verschwindet, wäre dies nur unter Energieaufwand möglich. Ohne Energiezufuhr ist die Drehung daher nicht möglich. Bei Doppelbindungen besteht keine freie Drehbarkeit.
|
Zur Lage der an die Doppelbindung gebundenen Atome gibt es die cis-trans Nomenklatur: |
WEITER: Dreifachbindung am C-Atom ZURÜCK: Einfachbindung am C-Atom ZURÜCK: Anfang "Kovalente Bindung"